kemi
Stoichiometris lagar beskriver de olika substansernas sammansättning, baserat på förhållandena (i massa) mellan varje art som intervenerar i reaktionen. All befintlig materia bildas av kombinationen, i olika proportioner, av de olika kemiska elementen som utgör det periodiska bordet. Dessa fackförbund regleras av vissa lagar av kombination som kallas "stoichiometrys lagar" eller "kemiets viktiga lagar". Dess
Etanamid är ett kemiskt ämne som tillhör gruppen organiska kväveföreningar. Den får också namnet acetamid enligt International Union of Clean and Applied Chemistry (IUPAC för dess akronym på engelska). Kommersiellt kallas det ättiksyraamid. Det kallas amid eftersom kvävet är fäst vid en karbonylgrupp. Det är prim
Maillardreaktionen är namnet på kemiska reaktioner mellan aminosyror och reducerande sockerarter som döljer mat under rostning, bakning, rostning och stekning. Bruna föreningar bildas ansvariga för färg och arom av produkter som brödskorpa, rostbiff, pommes frites och bakade kakor. Reaktionen gynnas av värmen (temperaturer mellan 140 och 165 ° C), även om den också sker vid lägre hastighet vid rumstemperatur. Det var de
Aluminiumklorid eller aluminiumtriklorid (AlCl 3 ) är ett binärt salt bildat av aluminium och klor. Ibland förefaller det som ett gult pulver eftersom det har föroreningar på grund av närvaron av järn (III) klorid. Det erhålls genom att kombinera dess element. Aluminium, som har tre elektroner på sin sista energinivå (familj IIIA), tenderar att ge dem på grund av metallets karaktär. Klor med s
Karboxylsyran är en term som tillskrivs vilken organisk förening som helst som innehåller en karboxylgrupp. De kan också kallas organiska syror och finns i många naturliga källor. Myrsyra, en karboxylsyra, destilleras exempelvis från myror och andra insekter, såsom bägaren galerita. Det vill säga en anthill är en rik källa till myrsyra. Även ättik
Alendronsyra är en organisk förening som tillhör klassificeringen av bisfosfonater, speciellt andra generationens Dessa är de som innehåller kväveatomer. Denna förening, liksom resten av bisfosfonaterna, har en hög strukturell analogi med oorganiskt pyrofosfat (PPi). Oorganiskt pyrofosfat är en produkt av många syntetiska reaktioner i kroppen. Det lagr
Myrsyra eller metansyra Det är den enklaste och minsta förening av alla organiska syror. Det är också känt som metansyra och dess molekylformel är HCOOH, med bara en väteatom bunden till kolatomen. Dess namn härstammar från ordet formica , vilket på latin betyder ant. Femtonde århundradet naturalister fann att vissa typer av insekter (formicidae), såsom myror, termiter, bin och skalbaggar, utsöndrar denna förening som ansvarar för sina smärtsamma bett. Även dessa ins
Vinsyra är en organisk förening vars molekylformel är COOH (CHOH) 2COOH. Den har två karboxylgrupper; det vill säga det kan släppa två protoner (H +). Med andra ord är det en diprotisk syra. Det kan också klassificeras som en aldersyra (surt socker) och ett bärnstensyraderivat. Dess salt är känt från tidig sort och är en av biprodukternas vinproduktion. Detta krista
Kalciumklorid (CaCl2 ) Det är ett oorganiskt salt bestående av kalcium, jordalkalimetall och klorhalogen. I den föreningen finns det flera elektrostatiska interaktioner som definierar kristallets yttre utseende och resten av deras fysikaliska egenskaper. Dessutom åtföljs det alltid av vattenmolekyler, som bildar hydrater med allmänna formler CaCl2 · xH20 med x = 0, 1, 2, 4 och 6. När x
Den exoterma reaktionen är en typ av kemisk reaktion där en energiöverföring sker, huvudsakligen i form av värme eller ljus. Namnet kommer från det grekiska prefixet exo , vilket betyder "till utsidan"; och termen "termisk", som avser värme eller temperatur. I detta avseende kan exoterma reaktioner överföra andra typer av energi till miljön där de genereras, t.ex. med ex
Kemiska lösningar är så kallade homogena blandningar i kemi. De är stabila blandningar av två eller flera ämnen i vilka ett ämne (kallat ett lösningsmedel) löses upp i ett annat (kallat ett lösningsmedel). Lösningarna antar lösningsmedlets fas i blandningen och kan existera i fasta, flytande och gasformiga faser. I naturen
Pyrolysen består av en termisk sönderdelningsprocess där ämnena - av organiskt ursprung i sin stora majoritet - utsätts för höga temperaturer i ett inert medium (utan närvaro av syre). När organisk material behandlas med hjälp av pyrolys erhålls produkter som används inom industriområdet. Ett av de e
Termokemi är ansvarig för undersökningen av de kaloriförändringar som utförs i reaktionerna mellan två eller flera arter. Det anses vara en viktig del av termodynamiken, som studerar omvandlingen av värme och andra typer av energi för att förstå hur processer utvecklas och hur deras energi varierar. Det är oc
Kaliumnitrat är ett ternärt salt bestående av kalium, alkalimetall och oxoanionnitrat. Dess kemiska formel är KNO 3 , vilket innebär att för varje K + jon finns en NO 3- jon - interagerar med den. Därför är det ett jonsalt och utgör en av alkalititraten (LiNO3, NaNO3, RbNO3 ...). KNO 3 är ett starkt oxidationsmedel på grund av närvaron av nitratanjonen. Det betyder
Difenylamin är en organisk förening vars kemiska formel är (C6H5) 2NH. Dess namn indikerar att det är en amin, liksom dess formel (-NH 2 ). Å andra sidan avser uttrycket "difenyl" närvaron av två aromatiska ringar kopplade till kväve. Difenylamin är följaktligen en aromatisk amin. Inom vär
Strontiumklorid är en oorganisk förening bildad av strontium, jordalkalimetall (Mr Becamgbara) och halogenklorid. Eftersom båda elementen har mycket olika elektronegativiteter är föreningen en jonisk fast substans vars kemiska formel är SrCl2. Eftersom det är ett joniskt fastämne utgör det joner. För fal
Fenolftalin är ett organiskt färgämne, vilket i sin tur är en svag diprotisk syra, som används i många volymetriska bestämningar som en syrabasindikator. Det är, om det är en diprotisk syra, i lösning kan det förlora två H + joner, och för att vara en indikator måste den ha egenskapen att vara färgrik i det pH-område som utvärderas. I basmedium (pH
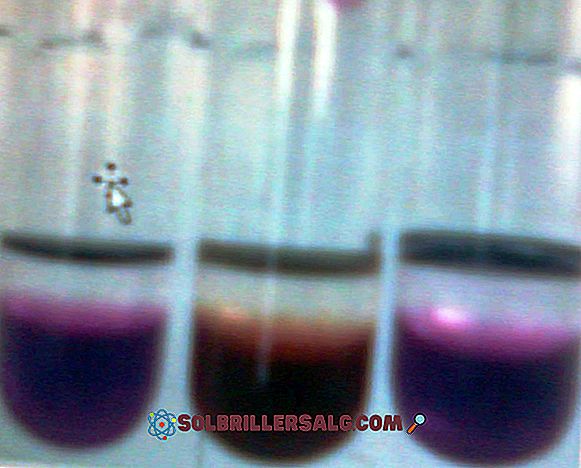
Kaliumpermanganat (KMnO4 ) är en oorganisk förening bildad av mangan-övergångsmetallgrupp 7 (VIIB), syre och kalium. Det är ett mörkt lila glasögonat fastämne. Deras vattenhaltiga lösningar är också mörka lila; Dessa lösningar blir mindre violetta eftersom de späds i större mängder vatten. KMnO 4 börjar
Strontiumoxid , vars kemiska formel är SrO (inte förväxlas med strontiumperoxid, som är SrO2), är produkten av den oxidativa reaktionen mellan denna metall och det syre som är närvarande i luften vid rumstemperatur: 2Sr (s) + O2 (g) → 2SrO (s). En bit strontium brinner i kontakt med luften som en följd av dess höga reaktivitet och eftersom den har en elektronisk konfiguration av ns2-typen, ger den lätt sina två valenselektroner, speciellt den syrediatomiska molekylen. Om metallet
Differensialen eller differentieringselektronen är den sista elektronen placerad i sekvensen av en atoms elektroniska konfiguration. Varför heter han? För att svara på denna fråga är en atoms grundläggande struktur nödvändig: dess kärna, vakuum och elektroner. Kärnan är ett tätt, kompakt aggregat av positiva partiklar som kallas protoner, och av neutrala partiklar kallas neutroner. Protonerna
Hydroxiapatit är ett kalciumfosfatmineral, vars kemiska formel är Ca 10 (PO 4 ) 6 (OH) 2 . Tillsammans med andra mineraler och organiskt material kvarstår krossat och komprimerat, bildar det det råmaterial som kallas fosforgaller. Uttrycket "hydroxi" avser OH-anionen. Om istället för det anjonet var fluor, skulle mineralet kallas fluorapatit (Ca 10 (PO 4 ) 6 (F) 2 , och så med andra anjoner (Cl-, Br-, CO 3 2-, etc.)., hy
Magnesiumfosfat är en term som används för att hänvisa till en familj av oorganiska föreningar som bildas av magnesium, jordalkalimetall och oxoanionfosfat. Det enklaste magnesiumfosfatet har den kemiska formeln Mg3 (PO4) 2 . Formeln indikerar att för varje två anjoner PO 4 3- finns tre Mg2 + -katjoner som interagerar med dessa. Dessa
Pyrexglas är ett speciellt borsilikatglas vars varumärke (Pyrex) har utseendet i New York 1915, tillverkat av Corning Glass. Det framkom som ett material för modern matförpackning, som också används för att lagra och baka mat i samma typ av behållare. Ursprunget av ordet Pyrex har genererat vissa skillnader, men det är accepterat att det härrör från den mest sålda artikeln i de första momenten av sin kommersialisering: en tallrik där en tårta bakades. Med detta glas
Enantiomerer är de par organiska (och oorganiska) föreningar som består av två spegelbilder som inte kan överlappa varandra över varandra. När motsatsen uppstår, till exempel, i fallet med en boll, en golfklubb eller en gaffel, sägs de vara achirala föremål. Begreppet chiralitet gjordes av William Thomson (Lord Kelvin), som definierade att ett objekt är chiralt om det inte kan överlappa med sin spegelbild. Händerna är
Icke-järnmetaller är alla de som saknar eller har försumliga mängder järn. Dessa, i olika massproportioner, används för att skapa legeringar som uppvisar bättre fysikaliska egenskaper än enskilda metaller. Sålunda är dess kristallina strukturer och metallinteraktioner hörnstenen i tillämpningarna av icke-järnlegeringar. Dessa rena m
Nedbörd eller kemisk utfällning är en process som består av bildning av ett olösligt fast ämne ur blandningen av två homogena lösningar. Till skillnad från nederbörd av regn och snö, i denna typ av nederbörd "regnar det fast" från vätskans yta. I två homogena lösningar löses joner i vatten. När dessa inter
Den metalliska karaktären hos elementen i det periodiska tabellen avser alla de variabler, kemiska och fysiska, som definierar metaller eller skiljer dem från andra naturliga ämnen. De är i allmänhet lätta, täta, hårda fasta ämnen, med höga värme- och elektriska ledningsförmåga, formbara och duktila. Emellertid
Diazoniumsalterna är organiska föreningar i vilka det finns joniska interaktioner mellan azo-gruppen (-N2 +) och en anjon X- (Cl-, F-, CH3COO-, etc.). Dess allmänna kemiska formel är RN2 + X-, och i detta kan sidokedjan R antingen vara en alifatisk grupp eller en arylgrupp; det vill säga en aromatisk ring. Str
Järnmetaller är de som innehåller järn (Fe), liksom små mängder andra metaller som tillsätts för att ge vissa fördelaktiga egenskaper till deras legeringar. Även om järn kan existera i olika oxidationstillstånd är +2 (järn) och +3 (ferris) de vanligaste. Uttrycket "järnhaltigt" avser emellertid närvaron av järn oavsett oxidationstillståndet i materialet. Järn är det fjär
Bandteori är en som definierar den solida elektroniska strukturen som helhet. Det kan appliceras på alla typer av fasta ämnen, men det är i metallerna där dess största framgångar återspeglas. Enligt denna teori härrör metallbindningen från den elektrostatiska attraktionen mellan de positivt laddade joner och de mobila elektronerna i kristallen. Därför ha